Пгд (предимплантационная генетическая диагностика)
Содержание:
- Цель обследования
- Как передаются по наследству генетические заболевания
- Методы проведения
- Что такое ПГД
- Как часто встречаются генетические отклонения у эмбрионов?
- Проведение предимплантационной генетической диагностики (обследование бластомеров)
- Как делают ПГД при ЭКО
- Стадии диагностики
- ПРЕИМУЩЕСТВА предимплантационной диагностики:
- Когда нужно делать ПГД
- Показания к преимплантационной генетической диагностики
- Показания для ПГД эмбриона
- Показания к проведению генетической диагностики эмбриона
- Полезная информация
- ПГД рекомендовано:
- Техника выполнения ПГД
- Оборудование для проведения безопасного ПГД
- Точность предимплантационной диагностики
- Стоимость преимплантационной генетической диагностики
- 17 ответов
Цель обследования
ПГД настоятельно рекомендуется родителям, у которых есть генетические заболевания, которые могут быть унаследованы малышом. Также такая предварительная генетическая экспертиза эмбрионов не помешает, если в рядах близких родственников будущих родителей были наследственные недуги.

Диагностика перед имплантацией важна и необходима парам, в которых кто-то из родителей является носителем заболевания, сцепленного с половой хромосомой. Например, женщина носит ген гемофилии, но больным ребенок будет только в том случае, если это будет малыш мужского пола. ПГД в этом случае определяет пол эмбрионов, которым всего несколько дней, и врачи отбирают для подсадки только тех зародышей, которым гемофилия не угрожает, то есть девочек.
Женщине с отрицательным резус-фактором и несколькими беременностями в прошлом (не имеет значения, чем они закончились), рекомендуется ПГД, если для экстракорпорального оплодотворения использовалась сперма мужа с положительным резус-фактором. В этом случае врачи отберут из всех получившихся зародышей только тех, кто унаследовал материнскую резус-принадлежность. В этом случае беременность после ЭКО протекать будет с меньшими рисками, и малышу не будет угрожать опасная гемолитическая болезнь.

ПГД рекомендуется паре в том случае, если у женщины было два и более выкидыша ранее, если имели место быть случаи замершей беременности, а также в том случае, если у любого из супругов в первом браке или у них совместно уже рождался ребенок с хромосомными аномалиями или генетическими патологиями. Диагностика до переноса позволяет исключить из числа рассматриваемых к пересадке зародышей тех, кто болен или имеет аномалии негенетического происхождения.

И совсем нестандартная, но, увы, реальная ситуация – родители идут на ЭКО, чтобы родить малыша, который сможет стать донором, например, костного мозга, для собственного старшего братика или сестры. В этом случае полагаться за естественное зачатие слишком рискованно. Родившийся ребенок может не подойти в качестве донора для больного родственника.
Предимплантационная диагностика поможет отобрать из получившихся эмбрионов особи с определенным сочетанием генетической информации, гарантирующей геномное совпадение между детьми. Это исследование называется HLA-типирование.

Как передаются по наследству генетические заболевания
В диаграммах ниже, D или d представляет дефектный ген, а N или n представляет нормальный ген. Мутации не всегда приводят к болезни.
Доминантные заболевания:
Один из родителей имеет один дефектный ген, который доминирует над своей нормальной парой. Так как потомки наследуют половину своего генетического материала от каждого из родителей, есть 50% риск наследования дефектного гена, и, следовательно, заболевания.

Рецессивные заболевания:
Оба родителя являются носителями одного дефектного гена, но при этом имеют нормальную пару гена. Для наследования заболевания необходимы две дефектных копии гена. Каждый потомок имеет 50% шанс быть носителем, и 25% шанс унаследовать заболевание.

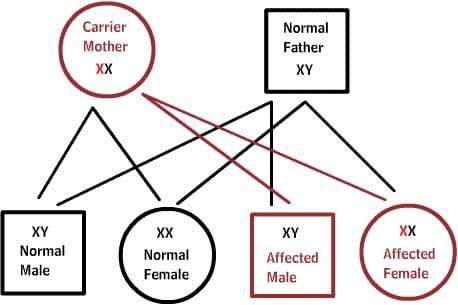
X-сцепленные заболевания:
Нормальные женщины имеют XX хромосомы, а нормальные мужчины XY. Женщины, которые имеют нормальный ген на одной из Х-хромосом, защищены от дефектного гена на их другой Х-хромосоме. Однако, у мужчины отсутствует такая защита в связи с наличием только одной Х-хромосомы. Каждый мужской потомок от матери, которая несет в себе дефект, имеет 50% шанс унаследовать дефектный ген и заболевание. Каждый женский потомок имеет 50% шанс быть носителем, как и ее мать. (на рисунке ниже X представляет нормальный ген а X представляет дефектный ген)
Методы проведения
На сегодня существует 4 метода проведения генетической диагностики эмбриона перед его имплантацией.
И для каждого из них необходимо соответствующее оснащение в помещении, где проводят процедуру.
FISH
Время проведения процедуры всего 4–5 часов. За этот период удается определить последовательность ДНК хромосом, а также получить данные о поле ребенка, выявить наиболее часто встречающиеся аномалии и найти эмбрионы с хромосомными перестройками.
CGH (сравнительная геномная гибридизация)
Времени на этот метод исследования затрачивается довольно много, зато можно проверить все хромосомы. Стоимость его в разы выше предыдущего способа диагностики.
Способ имеет ряд преимуществ:
- помогает выявить зародыши с наиболее высоким потенциалом к имплантации;
- значительно снижается риск неправильной постановки диагноза, что обусловлено проверкой большого количества стволовых клеток;
- диагностика проводится с замороженными бластоцистами, перенос которых в дальнейшем осуществляют в криопротоколе.
PCR
Полимеразная цепная реакция (ПЦР) выявляет нарушения в работе хромосом и наличие моногенных патологий, а также позволяет найти антитела HLA (антигены тканевой несовместимости родителей) и определяет принадлежность зародышей по резусу.
Перед проведением методики родителей и их близких родственников проверяют на наличие генных мутаций. Это позволяет более точно определить заболевание, возникающее вследствие доминантных и рецессивных аномальных изменений клеток. Если ЭКО проводится с донорской яйцеклеткой (ДЯ), методика ПЦР не подходит.
NGS
Эта современная диагностика носит название Now-Generation Sequencing, что переводится как «высокопроизводительное секвенирование». Метод довольно дорогостоящий, но его эффективность в несколько раз превышает все предыдущие диагностики, поскольку позволяет сделать весь геномный анализ – исследовать не только все хромосомы, но и полиморфизмы и мутации в каком-либо участке хромосом.
Во время проведения NGS-диагностики проверяется последовательность ДНК, благодаря чему можно точно установить генетические отклонения.
Что такое ПГД
Хромосомный набор яйцеклетки или зародыша изучается в лабораторных условиях. Учитывая ранние сроки развития эмбриона, риск его травмирования сводится к 1%. Процедура назначается параллельно с основным лечением, предусмотренным протоколом. Однако для нее потребуется больше фолликулов, поэтому гормональная стимуляция яичников проводится в более интенсивном режиме.
Не все хромосомные мутации у родителей представляют опасность для здоровья их малыша. Развитие патологии напрямую зависит от признаков и комбинации генов у мамы и папы.
Различают два вида мутационных признаков: доминантный и рецессивный. Передача малышу доминантного мутирующего гена увеличивает риск патологии у ребенка на 50%. Если родители – носители рецессивного признака, то генетическая болезнь появится, когда малышу передадутся оба «больных» гена мамы и папы.
К тому же некоторые генетические патологии связаны с полом. Так, женская двадцать третья хромосомная пара выглядит как XX, мужская – как XY. Поэтому нарушения в одной хромосоме женщин не вызовет болезнь, так как вторая заблокирует ее действие. Здоровый рожденный ребенок продолжит «носительство» дефектной хромосомы.
У мужчин нет такой защиты, поэтому от них мальчики родятся с генетической патологией, а девочки в половине случаев станут носительницами «бракованной» хромосомы.
Итак, процедура экстракорпорального оплодотворения проводится совместно с ПГД для таких целей:
- «Не допустить» к подсадке эмбрионы, у которых выявлены дефектные гены;
- Выяснить причины, по которым предыдущие протоколы ЭКО закончились безрезультативно;
- Снизить риск рождения малыша с патологией от родителей-носителей;
- Определить пол малыша, исключив хромосомные аномалии по половой принадлежности;
- Выявить эмбрионы, у которых есть предрасположенность к патологиям генетического типа;
- «Найти» зародыш, оптимальный по HLA-системе с другими детьми из семьи, который сможет стать донором при их лечении;
- Снизить вероятность прерывания беременности на ранних сроках;
- Уменьшить возможность появления гемолитического заболевания;
- Выбрать один «идеальный» эмбрион, устранив возможность развития многоплодной беременности.
Генетическая диагностика позволяет выявить и исключить такие опасные патологии:
- Болезни Тея-Сакса;
- Серповидно-клеточную анемию;
- Болезнь Гоше;
- Болезнь Верднига-Гоффмана;
- Ретинобластому;
- Хорей Хантингтона;
- Синдром Дауна;
- Нейрофиброматоз;
- Гемофилию;
- Миопатию;
- Ахондроплазию;
- Фенилкетонурию;
- Синдром Альперса;
- Поликистоз почек;
- Мышечную дистрофию Дюшена;
- Пигментозный ретинит;
- Болезнь Геттингтона;
- Миодистрофию Дюшена;
- Муковисцидоз;
- Анемию Фанкони;
- Глухонемоту;
- Торсионную дистонию;
- Пузырчатку;
- Синдром Эдвардса.
Этот список не исчерпывается представленными патологиями: их более 150 видов.
Отметим, что зафиксированы случаи ложноотрицательных результатов. Дело в том, что некоторые методы исследования диагностируют только определенное количество хромосом. «Неучтенные» гены могут оказаться дефектными.
Иногда происходит мозаичное развитие мутаций. Во время исследования клетка диагностируется как здоровая, а мутация происходит в процессе ее развития.
Как часто встречаются генетические отклонения у эмбрионов?
У эмбрионов отличного и хорошего качества достаточно большой процент изменений кариотипа (анеуплоидий), которые не позволяют нормально развиваться в дальнейшем. С данными в цифрах можно ознакомиться в таблице 1.
Таблица 1. Качество бластоцист и качество генетического набора хромосом
| Качество бластоцисты | Отличное | Хорошее | Удовлетворительное | Неудовлетворительное |
| Процент эмбрионов с правильным набором хромосом (здоровых) | 56,4% | 42,8% | 39,1 | 25,5 |
| Частота анеуплоидий (аномальный набор хромосом) | 43,6% | 57,2% | 60,9% | 74,5% |
Можно сделать вывод, что в 25–39% случаев беременность могут дать эмбрионы удовлетворительного и неудовлетворительного качества, так как они генетически полностью «здоровы». Но для того чтобы их выявить, нужен анализ ПГД. Проведение диагностики на таких эмбрионах крайне затруднительно. Клеточного материала слишком мало и его достаточно трудно получить без ущерба для развивающегося организма. Риск остановки развития эмбрионов удовлетворительного и неудовлетворительного качества после биопсии очень высок. Чаще всего их не подвергают исследованию.
Проведение предимплантационной генетической диагностики (обследование бластомеров)
После соглашения на экстракорпоральное оплодотворение репродуктолог оценивает необходимость проведения ПГД супружеской паре. В случае наличия показаний партнеры могут согласить или отказаться от процедуры. Далее подписывается документ, подтверждающий разрешение на проведение обследования.

На третий день с момента оплодотворения эмбриона генетик берет одну из сформированных клеток-бластомеров для анализа. Считается, что для плода это не имеет последствий, поскольку все клетки взаимозаменяемы.
Специалист проводит исследование по одному из выбранных ранее направлений: изучение строения клетки под специальным флуоресцентным микроскопом, исследование ДНК, используя метод полимеразной цепной реакции, чтоб определить наличие мутации.
Исходя из результата, эмбрионы, имеющие аномалии, не будут использоваться в процессе имплантации. Выбираются здоровые и качественные. Далее одного из них или несколько переносят в полость матки матери.
При биопсии полярного тельца происходит обследование хромосомного набора матери. Проводится она в том случае, если по женской линии выявлено наличие генетически обусловленной патологии. Процедура позволяет определить, здорова ли яйцеклетка, которая будет использоваться для оплодотворения, не нарушив ее структуры. Если аномалии не выявлены, то ее можно использовать для оплодотворения и переноса в полость матки.
Существуют случаи, когда проводится скрининг полярных телец, а затем уже бластомеров. Это позволяет получить более достоверный результат. Схему, по которой будет проходить обследование, выбирает специалист-генетик.

Как делают ПГД при ЭКО
Все начинается с подготовки. Подготовка к диагностике представляет собой консультацию и обследование супругов, у которых имеются показания к ПГД. Врач расскажет о преимуществах и недостатках процедуры. Поскольку для исследования потребуется большое количество зрелых яйцеклеток, то стимуляция в протоколе будет интенсивнее, что может послужить возникновению синдрома гиперстимуляции. После обследования пары приступают непосредственно к самой диагностике.
Процедура делится на 8 этапов:
- Яйцеклетки извлекаются и оплодотворяются в лаборатории.
- Клетка развивается в течение 3-5 дней.
- Лаборантами отбираются самые жизнеспособные оплодотворенные яйцеклетки.
- Проводится биопсия. У зародыша извлекают клетки для анализа.
- Фиксируется бластомер.
- Проводится гибридизация.
- Формируется биоинформационный анализ. Полученные данные расшифровываются.
- Генетик проводит МГК (медико-генетическое консультирование пациента).
 После ПГД генетик отбирает «чистые» эмбрионы — они будут пригодны для трансфера. Зародыши с дефектными хромосомами пациентке не подсаживаются.
После ПГД генетик отбирает «чистые» эмбрионы — они будут пригодны для трансфера. Зародыши с дефектными хромосомами пациентке не подсаживаются.
Стадии диагностики
На первом этапе происходит стимулирование женщины гормонами и трансвагинальное извлечение яйцеклеток – по стандартному плану ЭКО. Введение сперматозоида в женскую клетку способом ИКСИ. Этот прием используется по причине необходимости отсеять сперматозоиды не принимающие участия в процессе ЭКО.
Проведение биопсии для ПГД с извлечением бластомера и его последующей фиксацией. На третий день от зародыша отсекают одну из сформировавшихся 8 клеток. Процедура производится с помощью механического, лазерного или химического способа. Клетки в этот период не дифференцированы и являются идентичными. У каждой из них есть полный набор генетического материала. Поэтому биопсия не мешает оставшейся группе клеток полноценно развиваться.
Проведение ПГД с помощью показанных методов. Исследование продолжается не более 2 дней. На 5-е сутки эмбрион больше не может оставаться в инкубаторе. Необходимо в кратчайшие сроки произвести анализ и представить результаты ПГД для осуществления переноса зародыша в матку матери.

ПРЕИМУЩЕСТВА предимплантационной диагностики:
- Выбор и перенос в матку только тех эмбрионов, которые не имеют хромосомных патологий
- Снижение риска рождения ребенка с определенными генетическими дефектами
- Снижение риска невынашивания (примерно в 2 раза)
- Снижение риска многоплодия (примерно в 2 раза)
- Увеличение шанса на успешную имплантацию (примерно на 10%)
- Увеличение шансов на благополучное рождение ребенка (примерно на 15-20%)
- РИСК при проведении предимплантационной диагностики:
- Риск случайного повреждения эмбриона (<1%)
- Ошибочная диагностика (до 10%)
- 3,5% вероятности того, что эмбрион с патологией будет диагностирован как нормальный
- 10% вероятности того, что здоровый эмбрион будет диагностирован как эмбрион с патологией
- Отмена переноса эмбрионов из-за того, что по результатам ПГД во всех эмбрионах будет обнаружена патология (до 20%)
ПГД проводится в ходе стандартного цикла экстракорпорального оплодотворения. При ПГД из эмбриона извлекают одну или две клетки, а затем проводят их генетический анализ методом FISH (fluorescent in situ hybridization) на анеуплоидии, транслокации и другие структурные патологии. Другой тип диагностики — полимеразная цепная реакция (ПЦР), которая применяется для диагностики моногенных заболеваний. ПЦР проходит в два этапа:
1) биопсия эмбриона и фиксация бластомера;
2) генетическая диагностика.
Когда нужно делать ПГД
Пройти предимплантационную генетическую диагностику предлагают не каждой паре, решившей сделать ЭКО. Существует ряд показаний, при которых эта процедура рекомендована.
А именно:
- У супругов есть «дефектные» хромосомы, имеются моногенные аномалии либо выявлена хромосомная перестройка.
- Возрастная пара (женщина старше 35 лет, мужчина — после 40 лет). Чем взрослее пара, тем вероятнее рождение малыша с генными аномалиями, даже если у супругов не наблюдаются «неисправные» хромосомы.
- Предыдущие беременности заканчивались смертью новорожденных из-за резус-конфликта.
- Исследование яйцеклеток и сперматозоидов выявило наличие дефектных ген и хромосом.
- Неудовлетворительный результат спермограммы. Выявлены серьезные нарушения, такие как азооспермия или олигозооспермия.
- В предыдущих протоколах ЭКО беременность не наступала.
- Беременность прерывалась на ранней стадии развития эмбриона.
 Чем старше пара, тем с большей необходимостью нужно делать ПГД.
Чем старше пара, тем с большей необходимостью нужно делать ПГД.
Поскольку список генетических заболеваний довольно внушительный, диагностику при ЭКО рекомендовано проводить всем пациенткам старше 35 лет. Возрастные изменения нередко грозят неприятными «неожиданностями» во время беременности, даже если зачатие произошло естественным путем.
Ускоренное старение женского организма и ПГД
Существуют ситуации, при которых женский организм «стареет» гораздо быстрее в биологическом смысле. Ускоренному старению женского организма способствуют определенные факторы. Вот некоторые из них:
- длительный прием сильнодействующих лекарственных средств;
- нездоровый образ в жизни в прошлом (курение, алкоголизм, наркомания);
- хронические заболевания;
- вредные условия работы;
- плохая экологическая обстановка.
ПГД также необходима, если:
- Необходимо получение определенных стволовых клеток для лечения других детей в семье.
- Мужчина и женщина являются близкими родственниками.
- Супруги получили долю радиационного облучения.
Стоимость протокола ЭКО с ПГД значительно выше, чем без процедуры, поэтому решение о проведении диагностики принимается пациенткой самостоятельно. Необходимо учитывать, что всего в 20-40% случаев подсадка эмбриона заканчивается беременностью (в зависимости от возраста пациентки).
 ПГД позволяет не только выявить генные мутации у зародыша, но и повысить вероятность успешной подсадки (до 70%, в зависимости от возраста).
ПГД позволяет не только выявить генные мутации у зародыша, но и повысить вероятность успешной подсадки (до 70%, в зависимости от возраста).
Показания к преимплантационной генетической диагностики
Преимплантационной генетической диагностики (ПГД) рекомендуется, когда пары имеют риск передачи известных генетических аномалий своим детям. Только здоровые и нормальные эмбрионы переносятся в матку матери, тем самым снижая риск наследования генетической аномалией и необходимость прерывания беременности (после положительного пренатальной диагностики).
Кому показано ПГД
- Пары с семейной историей Х-сцепленные нарушения (Пары с семейной историей Х-хромосомой заболевания имеют 25% риск появления больного эмбриона (половина эмбрионов мужского пола)
- Пары с хромосомными транслокаций, которые могут вызвать отсутствие имплантации, невынашивания беременности, или психические или физические нарушения у детей
- Носители аутосомно-рецессивных заболеваний (для носителей аутосомно-рецессивных заболеваний, риск для эмбриона составляет 25%.)
- Носители аутосомно-доминантный заболеваний (для носителей аутосомно-доминантным заболеванием, риск для эмбриона составляет 50%.)
Состояния, диагностируемые с помощью ПГД
ПГД используется для диагностики 3-х основных групп заболеваний:
(1) сцепленные с полом нарушения,
(2) дефекты одного гена, и
(3) хромосомные нарушения.
Заболевания, сцепленные с полом.
Заболевания, связанные с Х-хромосомой передаются ребенку от матери, которая является носителем. Они передаются ненормальной Х-хромосомой и проявляется у сыновей, которые не наследуют нормальную Х-хромосому от отца (наследуют Y хромосому). Поскольку Х-хромосома передается потомству / эмбриону от матери, то больные отцы имеют здоровых сыновей, но их дочери имеют 50% риск того, чтобы стать носителями заболевания при условии, что мать здорова. Сцепленные с полом рецессивные расстройства включают гемофилию, синдром ломкой Х, большинство нервно-мышечных дистрофий (в настоящее время известны> 900 нервно-мышечной дистрофии), а также сотни других заболеваний. Сцепленные с полом доминантные расстройства включают синдром Ретта, incontinentia pigmenti, pseudohyperparathyroidism и витамин D-резистентный рахит.
Одиночные дефекты гена
ПГД используется для идентификации отдельных генных дефектов, таких как муковисцидоз, болезнь Тея-Сакса, серповидно-клеточная анемия и болезнь Хантингтона. При таких заболеваниях, патология обнаруживается молекулярными методами диагностики с использованием полимеразной цепной реакции (ПЦР) амплификации ДНК из одной клетки. Несмотря на достигнутый прогресс не все моногенные заболевания легко диагностировать. Так муковисцидоз имеет несколько известных мутаций. Из них только 25 мутаций в настоящее время диагностируются. Поскольку большинство из этих редких мутаций не тестируется, родители без каких-либо клинических проявлений муковисцидоза все еще могут быть носителями. Т.е существует небольшая вероятность, что даже пройденного тестирования человек может быть носителем гена муковисцидоза.
ПГД может также использоваться, чтобы идентифицировать генетические мутации, такие как BRCA-1, который не вызывает конкретного заболевания, но увеличивает риск множества заболеваний.
Хромосомные расстройства
Последняя группа включает в себя хромосомные нарушения, в которых множество хромосомных перестроек, в том числе транслокаций, инверсий и делеций, могут быть обнаружены с помощью различных методик.
Показания для ПГД эмбриона
Причинами для назначения преимплантационной генетической диагностики эмбрионов являются следующие факторы.
Возраст женщины, превышающий 34 лет. В возрасте 30 лет вероятность хромосомных нарушений составляет 1 к 385. В 35 лет этот показатель уже составляет 1 к 179, в 40 лет — 1 к 63, в 45 лет — 1 к 19. Применение предимплантационной генетической диагностики при ЭКО показало наличие аномалий у 20% эмбрионов, взятых у женщин в возрасте 35-39 лет, а у пациенток старше 40 лет процент анеуплодных зародышей равен 40. Большая их часть при переносе или не имплантируются в матке вовсе, или не вынашивается. Это главная причина малого числа успешных беременностей и родов у пациенток в возрасте от 40 лет.
Возраст мужчины, превышающий 39 лет. Как и у женщин в мужском организме возрастные изменения также приводят к накоплению генетических ошибок. У мужчин старше 39 лет наблюдается снижение числа морфологически нормальных сперматозоидов в семени.
Рецидивирующее (привычное) невынашивание. Ненормальная упаковка хромосом в половых клетках мужчины и/или женщины в паре вызывает фатальные нарушения в некоторых эмбрионах. Это приводит к систематическим (повторяющимся) выкидышам.
Аутосомно-доминантные патологии. Такие заболевания затрагивают половину полученных эмбрионов. Пары с аутосомно-доминантными наследственными патологиями в семейном анамнезе страдают от них сами или являются их носителями.
Хромосомные патологии. К невозможности зачатия, имплантации или вынашивания эмбрионов приводят различные нарушения структуры хромосом. К типичным аномалиям этого типа относятся:
- Инверсии – поворот участка хромосомы на 180 градусов;
- Делеции – отсутствие у хромосомы одного или нескольких участков;
- Дупликации – повторение участка хромосомы;
- Транслокации – перенос участков с одной хромосомы на другую.
О транслокациях нужно сказать отдельно. Такие перестройки хромосом бывают двух типов:
- Робертсоновские – прикрепление хромосом друг к другу или смена их расположения;
- Взаимные и рецепторные — смена участками разных хромосом мест своего расположения.
Примерно у одного человека из 1 из 900 имеются робертсоновские транслокации с участием хромосом 13, 14, 15, 21, 22. 1 человека из 625 наблюдаются взаимные транслокации. Для их выявления проводится кариотипирование обоих партнеров. У семейных пар с хромосомными транслокациями могут быть выкидыши или дети с врожденными психическими или физиологическими нарушениями.
Если транслокация сбалансирована и не сопровождается отсутствием или избытком хромосомных участков, а разрыв в хромосоме не приводит к дисфункции генов, человек не страдает. Ее носитель может иметь сложные аномалии развития, связанные или не связанные с наследственной патологией. Если транслокация не сбалансирована, сопровождается отсутствием или недостатком хромосомного материала, ее носители не страдают, но у некоторых из них наблюдается сниженная фертильность. Однако, имеется вероятность ее передачи эмбриону, что может спровоцировать неудачную имплантацию, повторный выкидыш или рождение ребенка с врожденными нарушениями психики или физиологии.
При ЭКО ПГД эмбриона также назначается парам с повторными безуспешными попытками экстракорпорального оплодотворения, гендерно обусловленными патологиями (селекция по полу), генетическими мутациями и по социальным показаниям.
Сделайте первый шаг — запишитесь на прием к врачу!
Записаться на прием к врачу
Показания к проведению генетической диагностики эмбриона
Процедура ПГД рекомендована семейным парам и одиноким женщинам, проходящим процедуру ЭКО, в следующих случаях:
- При наличии у одного или обоих родителей серьезных наследственных заболеваний и высоком риске их передачи будущему ребенку. При этом у самих пациентов эти патологии могут никак не проявляться, если они являются лишь носителями дефективных генов.
- Если возраст матери превышает 35 лет, а отца – 39-40 лет. После этого возрастного порога в половых клетках родителей резко возрастает количество генетических ошибок. При зачатии их комбинации могут спровоцировать у будущего ребенка собственные врожденные нарушения, не связанные с наследуемыми от папы или мамы мутациями.
- При риске возникновения резус-конфликта – иммунного отторжения резус-отрицательной матери плода с положительным резус-фактором. В этом случае женская генетика несовместима с геномом ребенка. Ее организм вырабатывает антитела, которые при попадании в кровь эмбриона вызывают разрушение его красных кровяных телец. Обычно такой иммунный ответ формируется у матери в момент первых родов, когда ее кровь смешивается с кровью плода. При последующих беременностях уже выработанный иммунитет приводит к тяжелым поражениям и гибели эмбрионов.
- При наличии в яйцеклетках или сперматозоидах родителей хромосомных и генетических аномалий, обусловленных возрастом, воздействием внешних факторов (излучения, токсичных веществ и т. д.).
- При 2-х и более безуспешных предшествующих попыток ЭКО неясной этиологии, а также свыше 2 спонтанных абортов в анамнезе женщины, произошедших на ранних стадиях беременности.
- При выявлении серьезных аномалий спермы отца на спермограмме – отсутствия или малого количества сперматозоидов, их малоподвижности, большого числа клеток с нарушенной морфологией и т. д.
- При наличии у родителей ребенка с тяжелым заболеванием, требующим лечения стволовыми клетками. В этом случае рождение генетически совместимого с ним малыша (по системе HLA) может решить проблему донорства.
Генетическая диагностика болезней, проведенная перед экстракорпоральным оплодотворением, позволяет отказаться от пренатального исследования, которое несет больший риск здоровью матери и ее малыша.
Сделайте первый шаг запишитесь на прием к врачу!
Записаться на прием к врачу
Полезная информация
ПГД рекомендовано:
- При бесплодии, привычном невынашивании беременности
- При неоднократных неудачных попытках ЭКО
- При возрасте женщины старше 35 лет
- При наличии высокого риска передачи наследственных заболеваний
Техника выполнения ПГД
Для проведения преимплантационной генетической диагностики эмбрионам проводится биопсия на 3 день (биопсия бластомера) или на 5 день (биопсия трофэктодермы) их развития.
На третий день развития эмбрион, как правило, состоит из восьми бластомеров (клеток). Биопсия эмбриона на данной стадии представляет собой отделение одной клетки от эмбриона. При этом существует риск повреждения эмбриона, что влечет за собой снижение потенциала его дальнейшего развития. Кроме того, на этой стадии эмбрионы имеют высокий уровень мозаицизма (до 55%), то есть наличия хотя бы одной клетки, отличающейся по хромосомному набору (генетическому составу) от остальных, что обуславливает риск ложнопложительных и ложноотрицательных результатов диагностики.
Более распространенной в современной практике является биопсия эмбриона на пятый день развития. В этот момент эмбрион уже находится в стадии бластоцисты (ранней стадии развития зародыша), состоящей из двух слоев клеток: внутриклеточной массы и трофэктодермы. Впоследствии трофэктодерма участвует в образовании плаценты, а внутриклеточная масса — в образовании плода. В процессе биопсии эмбриолог с помощью микроинструментов забирает сразу несколько клеток трофэктодермы, внезародышевой ткани. Это существенно снижает риск повреждения эмбриона, риск наличия мозаицизма, получения ложноположительных и ложноотрицательных результатов исследования, обеспечивает безопасность процедуры и повышает точность диагностики.
Оборудование для проведения безопасного ПГД
В Доме Планирования Семьи отдается преимущество проведению биопсии эмбрионов на 5 день. Техника проведения такой биопсии требует от эмбриолога значительного опыта и наличия высококлассного оборудования в лаборатории.
Биопсия проводится экспертами-эмбриологами на современном и надежном оборудовании — инвертированном микроскопе Olympus, оснащенном микроманипуляторами Narishige и активным лазером OCTAX NaviLase. При проведении PGD этот лазер позволяет максимально точно и безопасно отделить одну или несколько клеток (биоптат) от эмбриона. OCTAX NaviLase минимизирует вредное воздействие на клетку за счет низкой инвазивности и минимального облучения, и является предметом гордости Эмбриологической лаборатории клиники.
Точность предимплантационной диагностики
Генетический анализ на хромосомный набор может выполняться разными методами, в числе которых метод FISH (флуоресцентная гибридизация in situ), aCGH (метод сравнительной геномной гибридизации) и NGS (метод полногеномного секвенирования). Наша Клиника использует только самые современные методы aCGH и NGS, обеспечивающие информативные и надежные результаты. Слаженная работа команды репродуктологов, эмбриологов и генетиков позволяет достичь высокий процент наступления беременности в Клинике.
Стоимость преимплантационной генетической диагностики
| Название | Цена |
| ПГД методом NGS за каждый образец (30 календарных дней) | 30387 руб. |
| ПГД методом NGS за каждый образец (7 рабочих дней) | 36000 руб. |
| ПГД методом NGS за каждый образец (1,5 рабочих дня) | 39999 руб. |
| Анализ дополнительного образцаот ПГД-эмбриона | 9996 руб. |
Указаны цены на самые востребованные услуги со скидкой 30%, которая действует при оплате наличными или банковской картой. Вы можете обслуживаться по полису ДМС, оплачивать отдельно каждый визит, заключить договор на программу ЭКО или внести депозит и получать услуги со скидкой. Услуги оказываются на основании заключенного договора.
Принимаются к оплате пластиковые карты MasterCard, VISA, Maestro, МИР. Также доступна бесконтактная оплата картами Apple Pay, Google Pay и Android Pay.
17 ответов
Не забывайте оценивать ответы врачей, помогите нам улучшить их, задавая дополнительные вопросы по теме этого вопроса.Также не забывайте благодарить врачей.
Наталья Петровнагенетик 2017-07-07 20:26
Здравствуйте,
seq(1-22, X) x2 — значит, что всех хромосом по две.
То есть, нормальный набор хромосом, пол женский.
Дарья 2019-05-14 18:51
Добрый день! У меня пришел такой же результат пгд эмбрина seq(1-22, X) x2
Правильно ли я поняла, что триплоидия у этого эмбриона исключена?
До этого два раза была триплоидия. Очень боюсь снова, что она снова повторится.
Заранее спасибо.
Наталья Петровнагенетик 2019-05-14 23:31
Здравствуйте,
триплоидии не обнаружено.
Но в зависимости от метода, триплоидия может иногда не определяться. Прочитайте комментарий в заключении.
Александра 2020-01-13 17:20
Добрый день! Пришел вот такой вот результат ПГД
mos seg (19) 1/ 1-22, x 2 — мозаичная форма мопосомии хромосомы 19. Что это такое? К чему стоит быть готовыми? Нигде не можем найти ответа. Подскажите, пожалуйста!
Наталья Петровнагенетик 2020-01-13 18:47
Здравствуйте,
это единственный эмбрион и вы планируете его переносить?Какие были показания к ПГД?
Александра 2020-01-13 18:54
Нет, есть ещё один, но без ПГД, был ещё один после ПГД (там была норма), была имплантация, но на этом все и закончилось. Хотя был эмбрион 5 аа (девочка). сейчас стоим перед выбором либо брать проверенный эмбрион с таким нарушением, либо делать ПГД последнему эмбриону. Помогите, пожалуйста, советом. Что у нас с этим эмбрионом?
Наталья Петровнагенетик 2020-01-13 19:08
Какие были показания к ПГД?
Александра 2020-01-13 19:13
Привычная невынашиваемость, выявлены полиморфизмы в гемостаз, после двух удачных беременностей, были выкидыши на 8, 4 неделях. У мужа тератозооспермия
Наталья Петровнагенетик 2020-01-13 19:29
Ничего из этого, по сути, не является показаниями к ПГД.
Честно говоря, ранние прерывания двух беременностей не является показанием к ЭКО. Разве что возраст критический и плохие репродуктивные прогнозы.
Вот такой результат с мозаицизмом не имеет однозначной интерпретации. Именно из-за возможности получать такой результат во многих странах ПГД вообще не применяют, а в большинстве применяют лишь при строгих показаниях.
Такой результат может означать:
1. Погрешность метода
2. Если же выявленная аномалия, действительно, есть, то беременность не будет развиваться.
Так что, можно на риск подсаживать этого эмбриона.
Или же оставить его на потом и подсадить того, что без ПГД.
Александра 2020-01-13 19:34
Правильно ли я понимаю, что либо это погрешность метода и все будет хорошо, либо, если что-то и есть, то беременность прервётся?
Наталья Петровнагенетик 2020-01-13 19:54
Если это погрешность — то не известно что.
Если мозаичная моносомия 19 хромосомы есть — то, скорее всего, прервется на раннем сроке.
Александра 2020-01-13 20:05
Наталья Петровнагенетик 2020-01-13 20:07
Пожалуйста!
Елена Зайцева 2020-03-20 14:30
Добрый день!
Поучила результат молекулярно-генетического исследования при неразвивающейся беременности.
Помогите, пожалуйста, расшифровать.
Результат: Молекулярно-генетический кариотип: upd(1-2, Х) х2 pat — выявлена однородительская дисомия отцовского происхождения.
Наталья Петровнагенетик 2020-03-20 14:46
Здравствуйте
Елена, Ваш вопрос не имеет отношения к ПГД.
Однородительская дисиомия это вид хромосомной аномалии не совместимой с жизнью.
Ирина 2020-11-06 15:41
Добрый день. Получили результат ПГТ на хромосомные аномалии. Mos seq(1-22), (X, Y) cx (мозаично-хаотичный эмбрион) к переносу не рекомендован. Что это за отклонение? Помогите, расшифровать.
Наталья Петровнагенетик 2020-11-06 15:56
Здравствуйте
Это значит, что обнаружены аномалии по многим хромосомам.